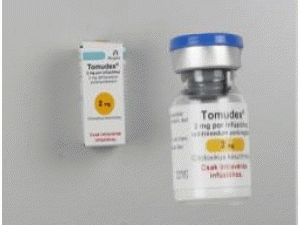
雷替曲塞冻干粉注射剂(Tomudex Trockensubstanz 2mg Vial)
 产地国家:澳大利亚
处方药:是
所属类别:2毫克/瓶 1瓶
包装规格:2毫克/瓶 1瓶
计价单位:瓶
生产厂家英文名:Hospira UK Ltd
原产地英文商品名:Tomudex Injection 2mg/vial 1vial
原产地英文药品名:Raltitrexed
中文参考商品译名:Tomudex冻干粉注射剂 2毫克/瓶
中文参考药品译名:雷替曲塞
产地国家:澳大利亚
处方药:是
所属类别:2毫克/瓶 1瓶
包装规格:2毫克/瓶 1瓶
计价单位:瓶
生产厂家英文名:Hospira UK Ltd
原产地英文商品名:Tomudex Injection 2mg/vial 1vial
原产地英文药品名:Raltitrexed
中文参考商品译名:Tomudex冻干粉注射剂 2毫克/瓶
中文参考药品译名:雷替曲塞
简介
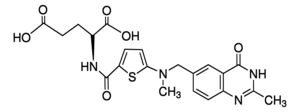
部份中雷替曲塞文处方资料(仅供参考) 英文药名:Raltitrexed Injection 商标名称:Tomudex 药物名称:雷替曲塞粉针 分子式成分:N-[5-[N-甲基-N-(2-甲基-4-氧代-3,4-二氢喹唑啉-6-基甲基)氨基]-2-噻吩甲酰基]-L-谷氨酸 制剂规格:本品为白色冻干粉末,每瓶含雷替曲塞2 mg。 药理学:研究表明,雷替曲塞为新一代水溶性胸苷酸合酶抑制剂,该药通过细胞膜外还原型叶酸盐载体系统将本品主动摄入细胞内,而后迅速代谢为多谷氨酸类化合物抑制胸苷酸合酶的活性,并能在细胞内潴留,长时间发挥作用。它对结肠直肠癌细胞系的抑制作用强于5-氟尿嘧啶,雷替曲塞的IC50长期给药为1.3~3.9nmol/L,短期给药为80nmol/L,而5-氟尿嘧啶与甲酰四氢叶酸合用长期给药IC50为330~5800nmol/L,短期给药为150000nmol/L。体外研究观察到雷替曲塞与5-氟尿嘧啶联合用药有协同作用,这种作用依赖于给药方案和剂量。 对176例晚期结肠直肠癌患者进行的II期临床试验,给予雷替曲塞3mg/m2,每3周1次,有25.6%产生综合疗效,从治疗到病情进展平均时间为4.2周,存活期平均为11.2月。1300多例晚期结肠直肠癌患者的3项III期临床研究结果表明,雷替曲塞治疗组(每3周1次,每次3mg/m2)与5-氟尿嘧啶加甲酰四氢叶酸治疗组(5-氟尿嘧啶425mg/m2加甲酰四氢叶酸20mg/m2或5-氟尿嘧啶400 mg/m2加甲酰四氢叶酸200mg/m2,每天1次,连续5天,每4~5周重复1次),所产生的客观有效率相似,分别为14.3%~19.3%和15.2%~18.1%,中位缓解时间分别为3.1~4.8和3.6~5.3个月,中位生存期分别为9.7~10.9和10.2~12.7个月。 药动学:患有不同程度实体瘤的患者给予本品3mg/m2治疗后,药物浓度与时间呈三室模型,Cmax的平均值为833μg/L,AUC为1090μg/L.h,分布相半衰期T1/2为0.8~3 h,最终消除半衰期T1/2γ为8.2~105h,与给药剂量无关。雷替曲塞主要消除途径是以原型药物形式从肾脏排出,患有轻、中度肾功能不全的患者的T1/2明显延长,AUC比正常肾功能患者增加2倍。 适应症:晚期直肠结肠癌的一线治疗。 不良反应:静脉滴注本品后常见副作用为血液毒性包括骨髓抑制,中性粒细胞减少、血小板减少等,胃肠道副作用有恶心、呕吐、腹泻,头痛、失眠、皮疹等现象,一般患者耐受性良好,副作用发生率较低。 相互作用:未见本品与华法林、非甾体抗炎药的相互作用,建议本品不与亚叶酸钙、叶酸和维生素制剂联合用药,以免发生相互作用,与其他细胞毒药物联合用药的安全尚未确立。 用法用量:推荐给药剂量为每次3mg/m2,用25至250ml0.9%生理盐水或5%葡萄糖稀释后静脉滴注15min以上,每3周重复给药1次。 药物过量:药物服用过量会产生严重的骨髓抑制等血液毒性和胃肠道毒性,应避免使用过量或遵医嘱,药物过量时可每6h给予亚叶酸钙25 mg/m2。 注意事项:对本品过敏者及有严重并发症者禁用。孕妇及哺辱期妇女禁用。本能只做单独给药,避免与其它药物混合使用。本品用0.9%生理盐水或5%葡萄糖水溶液稀释后应避光保存,在24小时内使用。轻度和中毒肝损伤患者使用时无需调整本品剂量,但本品部分经粪便排泄,严重肝损伤患者使用时应注意。 孕妇及哺辱期妇女禁用本品。儿童患者使用本品的安全性尚未确立,儿童慎用。老年患者用药药代动力学研究表明肾肾功能损伤的老年患者血浆清除率降低,可发生体内积蓄,应降低本品的剂量肌苷清除率在55~65mL/min,应给予推荐剂量的75%,肌苷清除率在25~54 mL/min,应给予推荐剂量的50%,每4周重复给药1次。英文版说明书
SOLUTIONLaboratórioAstrazenecaApresentação de TomudexPó liófilo parainfusão. emb. c/1 fr.-ampola de 2mg.Tomudex - IndicaçõesTratamento paliativo docâncer coloretalavançado. Contra-indicações de TomudexTomudex não deve serusado em gestantes, em mulheres que possam engravidar durante o tratamento ouque estejam amamentando. A possibilidade de gravidez deve ser excluída antes doinício do tratamento com Tomudex (ver item Uso durante a gravidez e lactação).Tomudex está contra-indicado para pacientes com in suficiênciarenalgrave. AdvertênciasRecomenda-se que Tomudex seja administrado apenas por ummédico, ou sob sua supervisão, o qual deve ter experiência em quimioterapiaantineoplásica e no tratamento dos efeitos tóxicos relacionados à quimioterapia.Os pacientes submetidos ao tratamento devem ser supervisionados apropriadamente,de modo que sinais de possíveis efeitos tóxicos ou reações adversas(particularmente diarréia) possam ser detectados e tratados imediatamente (veritem Posologia e Modo de Usar). Como outros agentes citotóxicos desse tipo, énecessário ter cautela em pacientes com função deprimida da medula óssea, malestado geral ou antes da radioterapia. Os pacientes idosos são mais vulneráveisaos efeitos tóxicos de Tomudex.Deve-se ter um extremo cuidado para assegurar amonitorização adequada das reações adversas, especialmente os sinais detoxicidade gastrointestinal (diarréia ou mucosite). Recomenda-se que a gestaçãoseja evitada durante otratamento e pelo menos por 6 meses depois do término dotratamento se um dos parceiros estiver recebendo Tomudex (ver item Uso durante agravidez e lactação).Uma proporção de Tomudex é excretada pelas fezes (ver itemFarmacocinética), portanto pacientes que apresentem insuficiência hepática levea moderada devem ser tratados com cautela.Não é recomendado o tratamento comTomudex em pacientes que apresentem insuficiência hepática grave. Tomudex é umagente citotóxico e deve ser manuseado de acordo com os procedimentos normaisadotados para esses agentes (ver item Instruções para uso e manuseio).Uso nagravidez de TomudexA gravidez deve ser evitada se um dos parceiros estiverrecebendo Tomudex. Recomenda-se também que a concepção seja evitada durante pelomenos 6 meses após término do tratamento. Tomudex não deve ser usado durante agestação nem em mulheres que possam engravidar durante o tratamento.Apossibilidade de gravidez deve ser excluída antes do início do tratamento comTomudex. Tomudex não deve ser administrado a mulheres que estejamamamentando.Interações medicamentosas de TomudexNão foram realizados estudosclínicos específicos de interações entre drogas. Leucovorina (ácido folínico),ácido fólico ou preparações vitamínicas contendo esses agentes, não devem serusa dosimediatamente antes ou durante a administração de Tomudex, porque podeminterferir em sua ação. Há estudos clínicos em andamento para avaliar o uso deTomudex em associação com outras terapias antineoplásicas. Tomudex apresenta 93%de ligação às proteínas plasmáticas e, embora tenha o potencial de interagir comdrogas que apresentam uma ligação protéica igualmente elevada, não foramobservadas interações de deslocamento com a varfarina in vitro. Os dados sugeremque a secreção tubular ativa possa contribuir para a excreção renal deraltitrexede, indicando uma interação potencial com outras drogas secretadasativamente, como antiinflamatórios não-esteroidais.Entretanto, a revisão dosdados de segurança dos estudos clínicos não revelou evidências de interaçõesclinicamente relevantes em pacientes tratados com Tomudex que também receberamantiinflamatórios não-esteroidais, varfarina e outras drogas geralmenteprescritas.Reações adversas/Efeitos colaterais de TomudexComo ocorre com outrasdrogas citotóxicas, Tomudex pode estar associado com certas reações adversas.Entre elas, incluem-se principalmente efeitos reversíveis normais用药温馨提示:当您服用此药物时,需定期接受医疗专业人士的检查,以便随时针对其药效、副作用等情况进行监测。本网站所包含的信息旨在为患者提供帮助,不能代替医学建议和治疗。
药品价格查询,专业药品查询网站,药品说明书查询,药品比价 » 雷替曲塞冻干粉注射剂(Tomudex Trockensubstanz 2mg Vial)
药品价格查询,专业药品查询网站,药品说明书查询,药品比价 » 雷替曲塞冻干粉注射剂(Tomudex Trockensubstanz 2mg Vial)